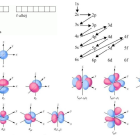
Egyenáramok

12.1. Faraday I. törvénye
1 mól, z vegyértékű anyag kiválasztásához ∙ töltés szükséges, ahol az F a Faraday számmal egyenlő. A Faraday szám azt adja meg, hogy mennyi töltés szükséges egy mól egy vegyértékű anyag kiválásához, tehát egyenlő az Avogadro állandó és az elemi töltés szorzatával

D
12.2. Faraday II. törvénye
Az elektrolízis során kiváló anyagok tömege egyenesen arányos az áthaladó töltésekkel. Hányadosuk az adott anyagra jellemző elektrokémiai egyenérték, ami az egységnyi áthaladó töltés esetén kiváló anyag tömegét adja meg g-ban.
Az elektrokémiai egyenérték azt adja meg, hogy mekkora töltés szükséges 1 mól, adott moláris tömegű, adott vegyértékű anyag előállításához.

13. Elektromos áram gázban, ütközési ionizáció
A gázok általában szigetelők, nagyrész molekulák alkotják, de kis százalékban kozmikus és földi eredetű sugárzás következtében mindig tartalmaz töltött részecskéket. Sugárzás hatására a molekulák ionizálódnak és elektron-ion párok alakulnak ki, melyek folyamatosan rekombinációja fenntartja a dinamikus egyensúlyt.
Elektromos tér hatására a gázban lévő elektron-ion párok nagy energiára tesznek szert, és ionizálják a semleges molekulákat, ütközések során elektron-ion párokat képeznek, létrejön az ütközési ionizáció, amely nagysága függ az elektromos tér erősségétől 1 / 2 2= , és a szabad út hossztól, hiszen minél nagyobb úton tud gyorsulni a töltéshordozó, annál nagyobb energiára tesz szert.
Az ütközési ionizáció kísérő jelensége a gáz fénykibocsátása. A fény színét a gáz anyagi minősége, erősségét a feszültség és a nyomás határozza meg. Normál nyomású gázokban/gázcsövekben, nagy feszültség hatására az elektródák környékén először ködfény és koronakisülés figyelhető meg, majd rövid ideig tartó elektromos szikra, ami átjut az anódról a katódra. Erre gyakorlati példa a villámlás, a szikrakisülés vagy a hegesztés ívkisülése.

14. Elektromos áram vákuumban:
Bizonyos ritkításnál (vákuum közeli állapot) újra fényjelenséget észlelünk, az üvegbúra anód felöli része zöldesen világítani kezd. Azt a fényt a katódból kilépő részecskék idézik elő. Ezt a katódból származó elektronkibocsátási folyamatot nevezzük katódsugárzásnak. 
14.1. Izzókatódos áramvezetés, Termikus emisszió
Izzókatódos áramvezetés negatív töltésű katód és pozitív töltésű anód között lép fel. A katódot fűtőszállal melegítjük, így a katód körül elektronfelhő jön létre. A katódból kilépő és a katódba belépő elektronok termikus egyensúlyban állnak, ami egy dinamikus egyensúly. Ha a katód közelébe pozitív töltésű anódot helyezünk, akkor elektronok szakadnak ki a katód elektronfelhőjéből, és jutnak át az anódra. A fűtősszállal történő gerjesztés miatt ezt nevezzük termikus emissziónak.
14.2. Fotokatód áramvezetése, Fotoemisszió
Fotokatód áramvezetése során a (vezető) katódból fény (vagy más elektromágneses hullám) hatására szakadnak ki elektronok, és ezek jutnak át az anódra.
14.3. Hideg emisszió
Hideg emisszió során erős elektromos tér szakít ki elektronokat a vezetőből. 
15. Elektromos áram felvezetőkben
15.1. Saját vezetés a félvezető kristályokban
A félvezetők (pl.: szilícium, germánium) kristályrácsa alacsony hőmérsékleten szigetelőnek számít, ám a vegyérték elektronok kristálybéli kötődése gyenge, hő vagy fény hatására elektronok szakadnak ki a kötésekből, elektron-lyuk párok jönnek létre, amely töltéshordozók száma adott hőmérsékleten folyamatos rekombináció mellet dinamikus egyensúlyi állapotba áll be, a hőmérséklet növekedésével exponenciálisan növekszik.
Lapozz a további részletekért