Atomfizika
4.1. Bohr posztulátumai
Az elektron bizonyos stacionárius pályákon nem sugároz. Ezen pályákra teljesül, hogy rajtuk az elektron impulzusmomentuma a ℏ egész számú többszöröse.
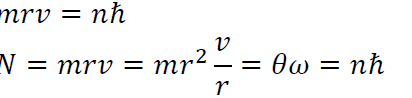 Az atom akkor bocsát kienergiát, ha az elektron egy magasabb energiájú stacionárius pályáról, egy mélyebb energiájú stacionárius pályára kerül, és energiaelnyelés közben mélyebb energiaállapotból magasabb energiaállapotba kerül. Az atom energiaelnyelése és kibocsátása is kvantumos
Az atom akkor bocsát kienergiát, ha az elektron egy magasabb energiájú stacionárius pályáról, egy mélyebb energiájú stacionárius pályára kerül, és energiaelnyelés közben mélyebb energiaállapotból magasabb energiaállapotba kerül. Az atom energiaelnyelése és kibocsátása is kvantumos 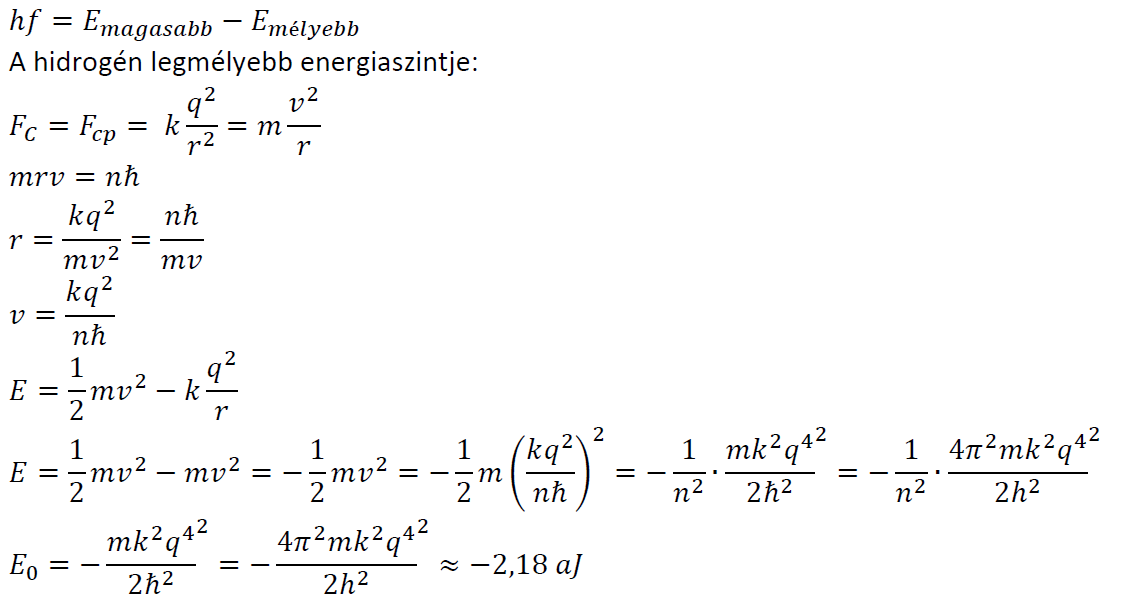

![]()
![]()
Magyarázat a hidrogén színképére
Az atom energiaelnyelése és kibocsátása is kvantumos. Az 1-es állapotba visszaérkező elektronok sugárzása az ultraibolya tartományba esik, elemeit a Lyman-sorozat adja meg. A 2-es állapotba viszszaérkező elektronok sugárzása a látható fény tartományba esik, elemeit a Balmer-sorozat adja 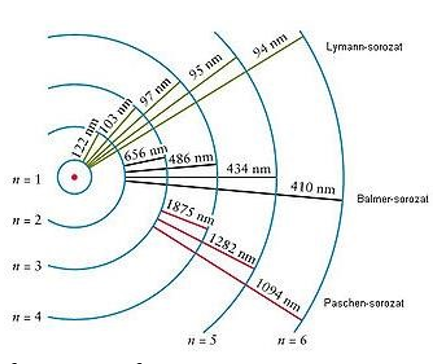

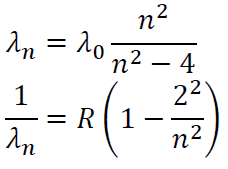
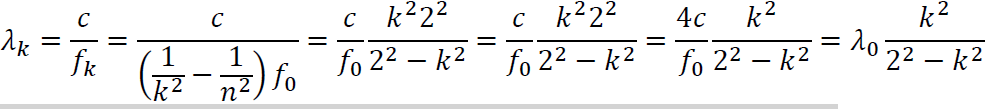
![]() A 3-es állapotba visszaérkező elektronok sugárzása az infravörös tartományba esik, elemeit a Paschen-sorozat adja meg.
A 3-es állapotba visszaérkező elektronok sugárzása az infravörös tartományba esik, elemeit a Paschen-sorozat adja meg.
4.2. Az elektron pályájának kapcsolata a de Broglie hullámhosszal
Az elektron pályáján a de Broglie hullámhossz egész számú többszöröse fér el, állóhullám alakul ki.
![]()
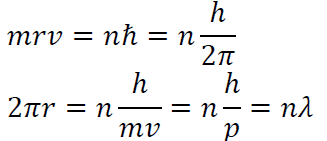
4.3. A Bohr modell eredményei és hiányosságai
A Bohr modell kiterjeszthető Z rendszámú atomra, de így csak egy elektronra alkalmazható.
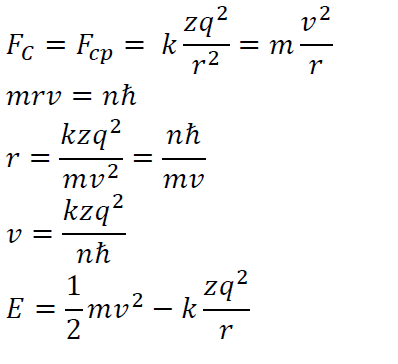
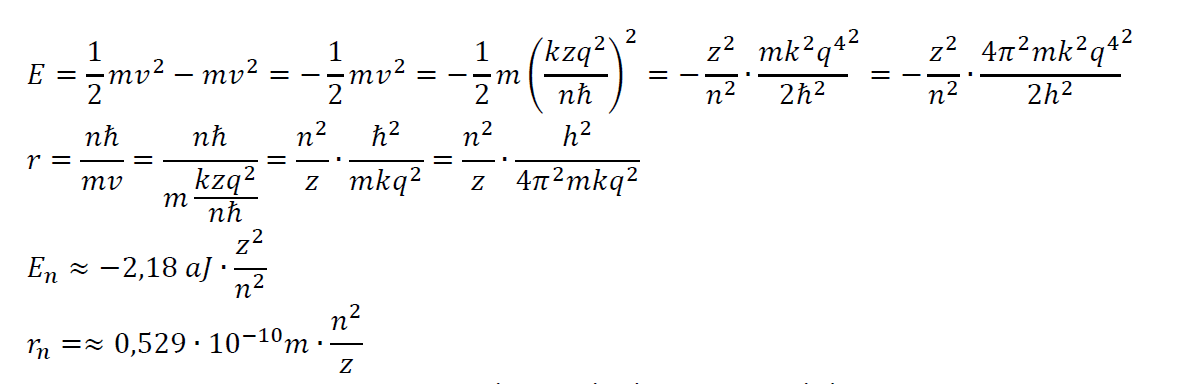 A Bohr modell nem tudta megmagyarázni a színképek felhasadását.
A Bohr modell nem tudta megmagyarázni a színképek felhasadását.
Nem tudta meg magyarázni az atomok közti kovalens kötést, és az atomok ütközéssel szembeni stabilitását.
5. A Bohr-Sommerfeld modell
Bohr és Sommerfeld az eredeti Bohr modellt azzal fejlesztették tovább, hogy a stacionárius pályák kör és ellipszis pályák lehetnek.
Az ellipszispálya nagytengelyét megadó összefüggés: 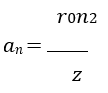 AZ ellipszispálya kistengelyét megadó összefüggés:
AZ ellipszispálya kistengelyét megadó összefüggés:
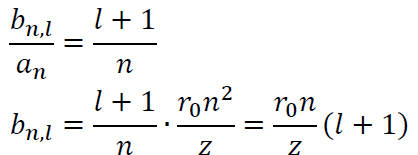
5.1. Kvantumszámok
a) Főkvantumszám
A főkvantumszám az elektronpálya energiáját határozza meg.
b) Mellékkvantumszám
A mellékkvantumszám az ellipszispálya méretét határozza meg.
c) Mágneses kvantumszám
A mágneses kvantumszám meghatározza, hogy az elektronpálya milyen irányba áll be a külső mágneses térhez képest.
d) Spin kvantumszám
A spin kvantumszám az elektron saját perdületét, spinjét adja meg.
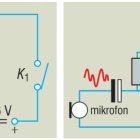
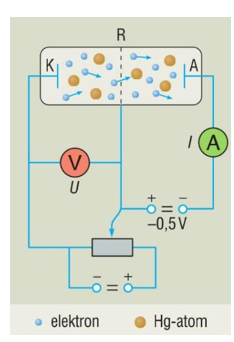
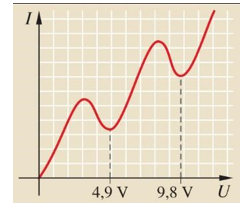
5.2. Franck-Hertz kísérlet
A kísérletben egy higanygőzzel töltött trióda katódjából termikus emisszióval elektronokat léptetnek ki. A katód és a rács közötti rácsfeszültség növelésével a kilépő elektronok képesek legyőzni a rács és az anód közé kapcsolt ellenfeszültséget, így az anódáram a rácsfeszültséggel együtt növekszik, ám egy a gőzre jellemző feszültségérték egész számú többszörösénél letörést észlelünk az áram-rácsfeszültség függvényben. Ennek oka, hogy az kilépő elektronok mozgási energiája eléri a higany kilépési munkáját és kilöki a higany mélyebb energiaállapotú elektronját, amelyet az egy magasabb energiájú elektronnal pótol, miközben sugároz. 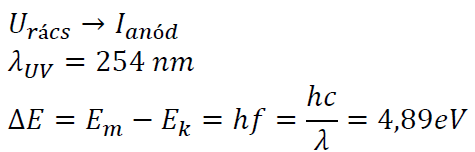
5.3. Karakterisztikus röntgensugárzás
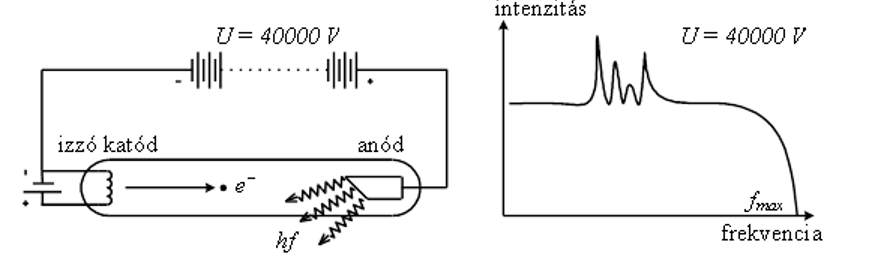
Vákuumdióda katódjából kilépő elektronok nikkel/molibdén anódon nyelődnek el, miközben az röntgensugárzást bocsát ki. A röntgensugárzás intenzitását a frekvencia függvényében ábrázoló grafikonon az adott anód anyagára jellemző helyeken kiugró intenzitásértékeket tapasztalunk. Az elektronok fékezési energiájából származik a grafikon egyenletes része. A kiugró értékek az anód anyagára jellemző, azon frekvenciaértékek esetén tapasztaljuk, amelyek az anód elektronjait kimozdítják a pályájukról.
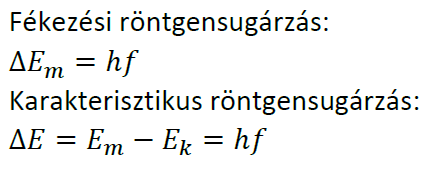
6. A kvantummechanikai atommodell
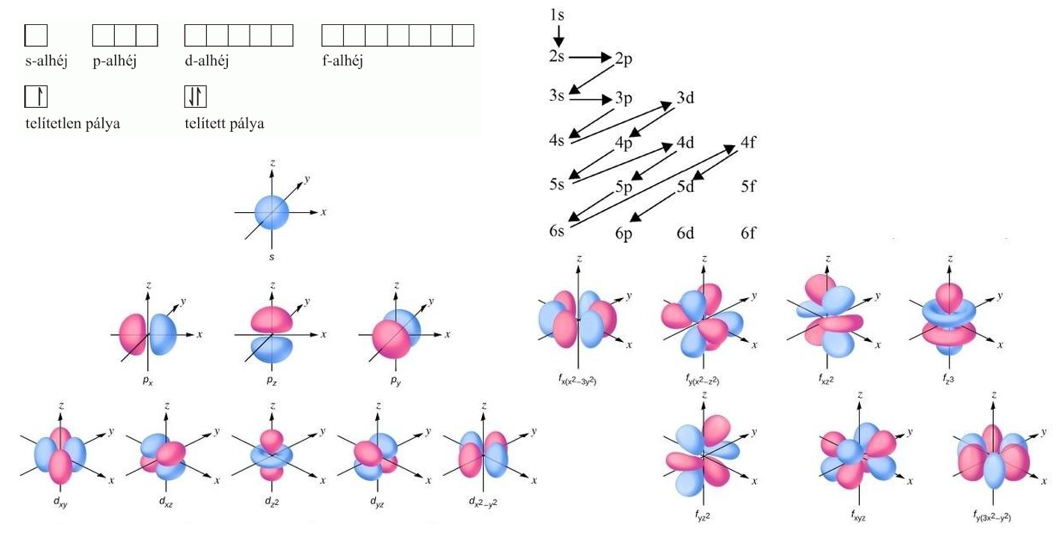
6.1. A kvantumszámok értelmezése
A Schrödinger kvantummechanikai atommodellje az elektronok atommag körüli állapotát megtalálási valószínűségi függvénnyel adja meg. Az elektronok megtalálási valószínűsége az atommag körüli bezárási tartományba háromdimenziós állóhullámokat alkot, vannak duzzadóhelyek viszonylag nagy megtalálási valószínűséggel, és olyan helyek is, ahol a megtalálási valószínűség értéke 0, ezek az állóhullám csomósíkjai. A levezetés során matematikai kényszerként adódó értékek a kvantumszámok.
a) Főkvantumszám
Az n főkvantumszám megadja, hogy egy elektronpályának hány csomófelülete van, értéke az elektron mozgási energiáját jellemzi. Az n értéke mindig pozitív egész szám. A növekvő főkvantumszámú pályák egyre messzebb vannak az atommagtól.
= 1, 2, 3,4 …
b) Mellékkvantumszám
Az l mellékkvantumszám megadja, hogy a csomófelületek közül hány csomósík van, értéke az elektronpálya alakját és impulzusát jellemzi. Az l értéke mindig nem negatív, egész szám, amely kisebb a főkvantumszámnál. A 0-s mellékkvantumszámú elektron S, az 1-es mellékkvantumszámú P, a 2-es mellékkvantumszámú D pályán található meg.
Lapozz a további részletekért