Az ATP (adenozin-trifoszfát)
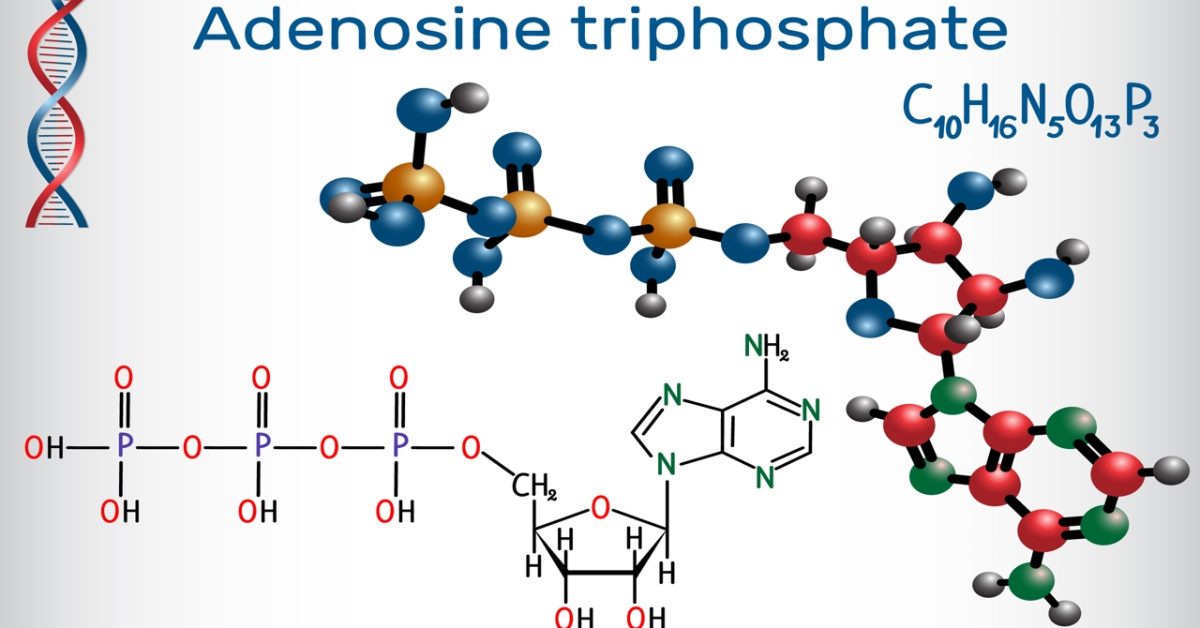
Adenozin-trifoszfát
Az adenozin-5′-trifoszfát (ATP) egy többfunkciós nukleotidszármazék, amely a sejten belüli energiaátvitel legkisebb molekuláris egysége. Az ATP a sejtek legfontosabb energiaraktározó vegyülete. Biológiai szerepe az energia tárolás és szállítás. Az ATP-t 1929-ben Karl Lohmann fedezte fel, majd 1941-ben Fritz Albert Lipmann feltételezte róla először, hogy ez a fő energiaszállító molekula a sejtekben
Az ATP kémiai energiát szállít a sejten belül az anyagcsere folyamataiban. Emberi szervezetben egyszerre csak kb. 250 g van jelen, de fokozott felhasználását jellemzi az, hogy naponta a testtömegnek megfelelő mennyiség fogy belőle. Ez úgy lehetséges, hogy az ATP folyamatosan újrahasznosúl. Jelentős izommunka esetén ez az érték akár fél kilogramm is lehet – percenként! Az energia a foszfátcsoportok közötti kötésekben raktározódik. Egy csoport leszakadásával átlag 30 kJ energia szabadul fel mólonként(ATP = ADP + P Q = 30 KJ/mol).
A fotoszintézis és a sejtlégzés folyamataiban energiaforrásként szerepel, és egy sor enzim és sejtfolyamat fogyasztja a bioszintetikus reakciók, a sejtmozgás és a sejtosztódás folyamataiban. Az ATP-t a nukleinsavakba is beépítik a polimerázok a DNS replikáció folyamatában és a transzkripcióban.
- A lebontó anyagcsere során felszabaduló energia nagy része ATP szintézisére fordítódik és így ATP formájában tárolódik.
- A felépítő folyamatokhoz szükséges energia viszont az ATP hidrolízisekor felszabaduló energiából származik
Az ATP növényi és állati sejtekben:
- A növényi sejtekben a legnagyobb mennyiségben a zöld színtestekben képződik ATP
- a fotoszintézis fényszakaszában.
- Az állati sejtekben a mitokondrium az ATP-előállítás fő színtere,
- s az ATP a terminális oxidáció folyamatában keletkezik.
- A terminális oxidáció során a mitokondrium belső membránjának két oldalán a hidrogénionok egyenlőtlen koncentrációja alakul ki.
- Az ATP-t előállító enzim a belső membránban található,
- amely a hidrogénionok koncentrációkülönbségének kiegyenlítődését teszi lehetővé, s az ennek során felszabaduló energiát építi be az ATP-be
ATP bontó enzimek
- A sejtmembrán általános ATP-bontó enzime a nátrium-kálium pumpa,
- amely a sejtekből nátriumionokat távolít el, ugyanakkor káliumionokat transzportál a sejtekbe,
- jelentős szerepet játszva ezzel a nyugalmi potenciál kialakításában.
- Idegsejtek esetén a nyugalmi potenciál az ingerlékenység alapfeltétele is.
- Az izomsejtek jellemző ATP-bontó fehérjéje a miozin,
- amelynek szerkezete ATP bontása során megváltozik (feji része konformációváltozást szenved, „bólint” / aktinmiozin komplex alakul ki),
- ennek során behúzza az aktinszálakat a miozinszálak közé, kiváltva ezzel az izomrostok összehúzódását.
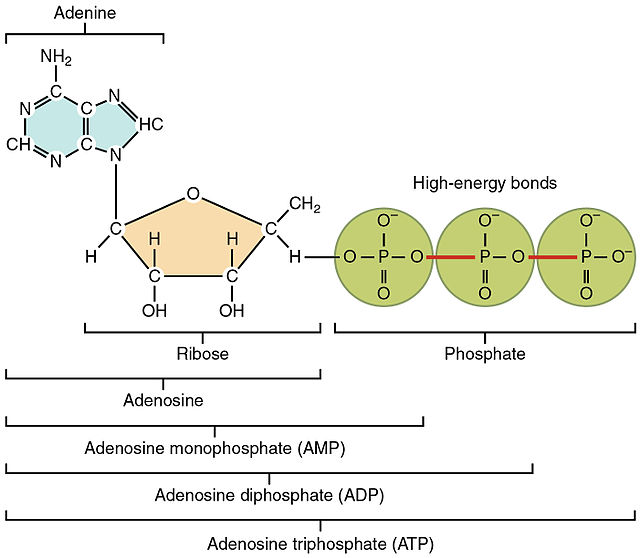
Az ATP nevének megfelelően – egy adenozinmolekulából és a hozzá kapcsolódó három foszfátcsoportból épül fel (ábra). A legutolsó foszfátcsoport leválasztása során már csak két foszfátcsoportot tartalmazó vegyület keletkezik: az adenozin-difoszfát (ADP). A foszfátcsoport lehasításakor igen nagy energia szabadul fel, amelyet a sejt kémiai folyamatainak sokasága képes felhasználni. Az ATP legnagyobb része a sejteken belül található mitokondriumokban képződik Az ATP-nek az ADP-ből való képzéséhez viszont ugyanígy nagy energiabefektetés szükséges, amelyet a sejtekben a cukrok és zsírsavak lebontása és oxidációja biztosít.
A folyamat a következőképpen zajlik: a légzés útján a sejtekhez jutott oxigén segítségével cukorégetés történik és a felszabaduló energia révén hidrogénion (proton) pumpálódik ki a membránon kívüli részbe. A protonok pozitív töltése miatt elektrokémiai potenciál különbség (pozitív töltéstöbblet) keletkezik.. A belső membrán két oldalán létrejött hidrogénion töltéskülönbség nyomán egy membránba beágyazott ATP-áz enzim, (amely egy olyan integráns tetramer membránfehérje, mely 2 alfa és 2 béta-glikoprotein alegységbıl áll) alfa részén (amely ion-csatornaként is működik) keresztül a protonok visszaáramlanak, és – mint amikor az áramló víz a vízimalom kerekét meghajtja – a felszabaduló energia segítségével ATP képzıdik ADP-ből és foszfátból oly módon, hogy a protonok áramlásának a hatására membránba ágyazott béta egység (szerepe a fehérje konformációjának és flexibilitásának szabályozása) egyik fehérjéjének korongja elfordul, és így az ehhez kapcsolódó – a mitokondrium belseje felé néző ATP-áz enzim másik fő része, a béta fehérjegombolyag egyik alegysége is körbefordul. Ugyanakkor a béta egység másik fehérjéje nem tud elfordulni (a membránhoz rögzül), így a középen újra és újra elforgó aszimmetrikus alegység körkörös elfordulást végez és ez változtatja meg az alegység kötőképességét, amely azután ADP-t és a foszfátiont ATP-vé kapcsolja össze a membrán belső oldalán. A legérdekesebb, hogy ezt a körforgást hidrogénionok áramlása tartja fenn, azaz az alfa forgástengelyen a béta egyik alegysége a hidrogénion-áramlástól hajtva „pörög”. Ez egy valódi forgó gépezet, az egymáson elcsúszva percenként többszázszor körbeforduló fehérjék mozgása végzi az ATP szintézisét.
Mindez az ATP-képződési és lebontási folyamat állandóan és nagy sebességgel folyik a szervezetünkben: a naponta képződő ATP mennyisége. Az adenozin-trifoszfát (ATP) és az adenozin-difoszfát (ADP) kémiai szerkezete. A vegyületek a sejten belül Mg2+-ionokkal alkotnak komplexet. az emberi testben, nyugalmi állapotban is 30–40 kilogramm (!), izommunka esetén azonban akár egy tonnányira is felmehet. Természetesen ez nem egy tonnányi új anyag képződését, hanem az ATP folyamatos szintézisekor és lebontásakor újra és újra feldolgozott mennyiséget jelenti. Viszont az így a képződő összes ATP mintegy harminc százalékát a nátrium–kálium pumpa használja fel. Az élő sejteken belüli ionösszetétel ugyanis jelentsen különbözik a sejteket körülvevő vérplazma vagy szöveti folyadék összetételétől. A sejten belüli viszonylag magas kálium-, ill. alacsony nátriumkoncentrációra az első magyarázat a sejthártya „átjárhatatlansága” volt ezekre a kationokra nézve. Később azonban kiderült, hogy a nátrium ill. a kálium mégiscsak viszonylag gyorsan kicserélődik a sejtek és környezetük között. Amiért az aktív transzport felelős. Maga a folyamat a nátrium-kálium pumpának köszönhető, amely e két iont a sejtmembránon keresztül ellentétes irányba mozgatja. A sejt membránpotenciáljának szinten tartásához, a sejtek a bennük lévő nátrium-ion koncentrációját alacsonyan, míg a kálium-ionét magasan tartják. A kivitelező az ATP-áz, a nátrium-kálium pumpa, amely 3 nátrium-iont pumpál ki a sejtből, míg 2 kálium-iont juttat be, eggyel csökkentve a sejtben lévő pozitív töltések számát. Arra is fény derült, hogy az ideg- és az izomszövet aktivitása során nátriumionok tömege áramlik be az ingerelt sejtekbe, míg e sejtek nyugalmi állapotában helyreáll a nátriumkoncentráció eredeti jelentős különbsége. A beáramlás révén jutnak be a sejtbe a fehérjék, a glükóz, vagy más tápanyagok, ugyanakkor viszont a felesleges nátrium ionokat később el is kell szállítani onnan.
Lapozz a további részletekért