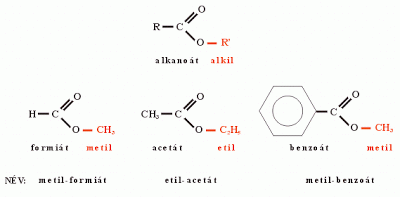
Karbonsavak és észterek

Homológsor: A telített, egyértékű észterek homológsorának összegképlete CnH2nO2 (n>3).
Fizikai tulajdonságok
- Hidrogénkötés kialakításában akceptor.
- A legkisebb vegyület standard halmazállapota folyadék (metil-formiát).
- Olvadás- és forráspont azonos (nem túl nagy szénatomszám esetén) az éterekénél magasabb (lévén gyenge dipólus-dipólus kölcsönhatás).
- Vízoldékonyság a kisebb molekulák esetén nem jó.
- A kismolekulájú vegyületeknél: különböző gyümölcsaromák (a nagy szénatomszámú, nem illékony képviselőik szagtalanok).
Hirdetés
Kémiai tulajdonságok
- Sav-bázis jelleg: A vizes oldat kémhatása semleges, hidrolízis esetén gyengén savas.
- Hidrolízis: lúgos közegben az észterek karbonsavra és alkoholra hidrolizálnak. Mivel a közeg lúgos, ezért a sav ionos formában lesz jelen a hidrolízis után: A hidrolízis során tehát gyakorlatilag sót (a karbonsav nátrium sóját) és alkoholt kaptunk. Ha a karbonsav sójának R-csoportja (alkil-csoport) nagy, úgy szappanokról beszélünk. Az észterek lúgos hidrolízisét szappanosításnak nevezzük.
- Oxidáció: csak erélyes körülmények között megy végbe.
- Ammóniával és aminokkal amidokat képeznek, ugyanis a reakció során karbonsav-amid (lásd ábra) és alkohol keletkezik. A folyamat hasonló, mint az észterhidrolízis, csak mivel az amid stabilisabb, mint az észter, az egyensúly gyakorlatilag teljesen az amidképzés irányába tolódik el.
Fontosabb észterek
- Zsírok és olajok (trigliceridek)Az acilező savak mindig páros szénatomszámúak, leggyakrabban OLAJSAV, PALMITINSAV, SZTEARINSAV. Az alkohol pedig a GLICERIN.
- Foszfatidok
- Gyümölcsészterek: Kis szénatomszámú alkánsavak egyszerű alkilésztere.
- Viaszok: Nagy és páros szénatomszámú, normál láncú, telített karbonsavak és ugyanilyen típusú alkoholok észterei! (pl. méhviasz)
Lapozz a további részletekért