Az elektron kettős természete
Az elektron felfedezése
– 1897 J. J. Thompson (1906 Nobel díj)
– megmérte a katódsugarat alkotó részecskék fajlagos töltését
folyamat:
– homogén mágneses térbe belépő töltött részecske körpályán mozog, tehát körmozgást végez illetve hat rá a Lorentz erő.
, ahol r körpálya sugara, v a részecske sebessége
(1)
-szükséges a részecske sebessége
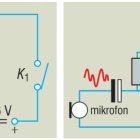
– Thompson elektromos és mágneses térbe vezette a katódsugarakat az alábbi módon:
Két kondenzátor lemez segítségével elektromos mezőt hozott létre, ezt egy tekercsbe tette, így mágneses mező is jelen volt. Úgy állította be az elektromos és a mágneses mező nagyságát, hogy a katódsugarak a két tér együttes hatása alatt ne térüljön el.
(E=, B=)
A kapott sebességet visszahelyettesítjük az (1)-es egyenletbe és a következőt kapjuk:
Katódsugárzásról igazolta, hogy negatív elektromos töltésű részecskékből áll, melyek 2000-szer kisebb tömegű, mint a hidrogénatom tömege.
– 1911 Millikan: elektron töltése e= 1,6 * 10^ -19 C és elektron tömege
m= 9,1 * 10^-31 kg
Millikan kísérlet
– vízszintes helyzetű kondenzátor lemezei közé apró (10-100 nanométer átmérőjű) olajcseppet porlasztott
– porlasztás közben egyes olajcseppek molekulái ionizálódtak
– erre az olajcseppre ható erők:
(= olaj sűrűsége, V olaj térfogata, = levegő/közeg sűrűsége)
() gravitációs erő:
() felhajtó erő:
() elektromos erő:
() közegellenállási erő:
Az elektromos tér az olajcseppet felgyorsítja, ezért a közegellenállási erő is növekszik. Egy idő után beáll egy állandó v sebesség tehát .
összegezve az erőket: += + (2)
Ha behelyettesítjük a fentebb leírt képleteket akkor: az olajcsepp sebességét meg tudjuk mérni, a q-t keressük és a sugarát egy másik összefüggésből meg tudjuk határozni (nem mérhető).
Sugár megállapítása: elektromos tér nincs bekapcsolva tehát = +
A kapott sugarat visszahelyettesítjük a (2)-es egyenletbe, ahol q-t kifejezzük.
Millikan szerint
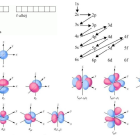
– Louis de Broglie hipotézise (mikrohullám hipotézis): a részecske-hullám kettős természet nem csak a fénynél van jelen, hanem a korpuszkuláris anyagokra is
– ez a feltételezés akkor lesz igaz, ha interferenciát lehet kimutatni
– ha a feltételezés igaz, akkor az elektronnak hullámhossza és frekvenciája is lesz
– de Broglie összefüggések (egyenletek) melyek egybefoglalják az elektron részecske és hullám jellemzőit is:
E= h*f, ahol E az energiája, h a Planck állandó (melynek értéke 6,626 * 10^ -27) és f a frekvencia.
p= h/λ, ahol p az impulzus, λ a hullámhossz.
– az elektron diffrakció jelensége például bizonyítja De Broglie hipotézisét
Első kísérleti bizonyítások
– C. Davidson és É. Germer: nikkelkristály felületéről csak bizonyos beesési szög esetén verődtek vissza az elektronnyalábok (1937 Nobel díj)
– ez volt az interferenciakísérlet mely bizonyítja az elektron hullámtermészetét
– G. P. Thomson : mikrokristályon keresztül az elektronnyalábok → fényérzékeny lemezen vagy fluoreszkáló ernyőn koncentrikus interferenciagyűrűket hoznak létre
– G. P. Thomson (J. J. Thomson fia): első tudatos elektronelhajlítás
Elektronmikroszkóp működés
– olyan mikroszkóp ahol nem fényt használnak a megfigyelendő tárgy megfigyelésére hanem felgyorsított elektronokat, elektronnyalábokat.
– miért jó: sokkal nagyobb felbontásban látszódik a tárgy
– „Az elektronágyúból származó elektronnyalábot vákuumcsőben inhomogén elektromos és mágneses terek gyorsítják, fókuszálják a mintára, az azon átjutó, elhajló, vagy egyéb kölcsönhatásból származó sugárzást megfelelő detektorokkal érzékelve készül a kép.”