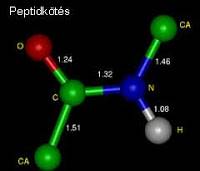
Szerves kémia
A szerves kémia a szénvegyületek kémiája. A szénatomok különleges tulajdonsága, hogy egymással kovalens kötést képezve elvileg korlátlan számú szénatom összekapcsolódhat láncokká, gyűrűkké.
Képletek írása: Egy szerves vegyület azonosításához nem elég az összegképletét felírni. Már a legegyszerűbb összegképletek is többféle anyagot jelenthetnek, például a C2H6O lehet egy éter vagy etil-alkohol képlete is. A szénatom a szerves vegyületekben mindig négy kovalens kötést képez.
Szerkezeti képletek: A szerkezeti vagy konstitúciós képlet megmutatja az atomok egymáshoz való kapcsolódásának a sorrendjét, de nem adja vissza a vegyület térszerkezetét. Az egyszerűsített vonalképletek esetén a vegyjeleket nem írjuk ki, csak vonalakat, ez a félkonstitúciós, vagy atomcsoportos képlet, például CH3-CH2-CH3.
A szénnek egyedülálló kémiai tulajdonságai vannak:
- kapcsolódni tud az összes többi elemhez
- hosszú láncokban tud saját magához kapcsolódni
- a szerves kémia változatossága lenyűgöző
- sok lehetséges molekulaszerkezet
- sok lehetséges reakció
Lewis-szerkezetek
- az oktett szabály – az atomok arra törekszenek, hogy 8 vegyérték-elektronjuk legyen (betöltött héjl)
- ionos kötés – elektronfelvétel vagy -leadás – az elektrosztatikus vonzás stabilizálja
- kovalens kötés – elektronmegosztás – a legáltalánosabb kötés a szerves molekulákban
Atompályák
- hullámfügvények – leírják az elektronok helyét
- s pályák (gömbölyű)
- p pályák (három: x,y,z) – (súlyzó alakú – 2 lebeny)
- d pályák (4 lebeny) – általában nem szükséges a szerves kémiához
- hibrid pályák – kombinált pályák
Hibrid pályák
- sp hibridek (egy s plusz egy p) – két azonos pályát ad (egyenes)
- sp2 hibridek (egy s plusz két p) – három azonos pályát ad (háromszög alakú)
- sp3 hibridek (egy s plusz három p) – négy azonos pályát ad (tetraéderes)
Kötés
- vonzás a negatív elektronok és a pozitív mag között – taszítás az elektronok között – taszítás a magok között
- a kötés a vonzóerők és a taszítóerők egyensúlya
- jellemző kötéstávolság és kötéserősség
Molekulapályák
- az atompályák átfedése
- az elektronok két mag közelében vannak
- kötő és nem kötő kombinációk
Szigma-kötések
- hengerszimmetria
- az atompályák végeinek átfedésével keletkezik
Pi-kötések
- a kötéstengelyen keresztül csomósík
- az atompályák oldalának átfedésével keletkezik
Szerves molekulák ábrázolása
- Lewis-képlet – minden elektront ábrázolunk
- Kekulé-képlet – a kötéseket vonalak jelölik – a magános elektronpárokat néha elhagyjuk
- vonalas képlet – elhagyjuk a magányos elektronpárokat – elhagyjuk a hidrogént a szénatomokon – elhagyjuk a szénatomokat (feltételezzük, hogy minden kötés végén szén van)
A kémiai szerkezet megjelenítése
- Név (triviális vagy szisztematikus)
- Tömör képlet (ahogy általában nyomtatva van)
- Lewis-képlet (az összes atom és kötés fel van tüntetve)
- Vonalas képlet (elhagyja a hidrogéneket; a szénatomokat a csúcsok jelentik)
- 3-D szerkezet (jelzi a kötések térbeli elhelyezkedését)
- Golyó és pálcika képlet (mit egy molekulamodell)
- Térkitöltéses modell (az elektroneloszlás teljes méretét közelíti)
Jellemző vegyérték
- H: 1 vegyérték-elektron, 1 kötés
- C: 4 vegyérték-elektron, 4 kötés
- N: 5 vegyérték-elektron, 3 kötés + 1 magános elektronpár
- O: 6 vegyérték-elektron, 2 kötés + 2 magános elektronpár
- F: 7 vegyérték-elektron, 1 kötés + 3 magános elektronpár
Molekulapályák
- H + H —> H-H
- s + s —> szigma-kötés
- H-H kötéshossz: 0,74 A
- H-H kötéserősség: 104 kcal/mol
Metán
- C + 4 H —> CH4
- sp3 + s —> négy szigma-kötés
- C-H kötéshossz: 1,10 A
- C-H kötéserősség: 104 kcal/mol
- elhelyezkedés – tetraéderes
- kötésszögek: 109,5o
Miért hibrid pályák?
- jó alak (irány)
- a kötésnél nagyfokú átfedés lehetséges
- maximális az elektronok sűrűsége az atomok között
- jó irányítottság
- minimális taszítás a pályák között
Etán
- CH3CH3
- egy C-C szigma-kötést tartalmaz
- sp3 – sp3 pályák átfedése
- C-C kötéshossz: 1,54 A
- C-C kötéserősség: 88 kcal/mol
- C-H kötéshossz: 1,10 A
- C-H kötéserősség: 98 kcal/mol
- irányítottság – két tetraéder
Etilén
- CH2=CH2
- egy C=C kettős kötést tartalmaz (alkén család)
- sp2 – sp2 pályák átfedése (szigma-kötés)
- p – p pályák átfedése (pi-kötés)
- C-C kötéshossz : 1,33 A
- C-C kötéserősség: 152 kcal/mol
- C-H kötéshossz: 1,08 A
- C-H kötéserősség: 103 kcal/mol
- irányítottság – sík
- kötésszög 120o
Acetilén
Lapozz a további részletekért