Amionósavak és fehérjék
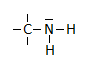
Az aminosavak
A fehérjék makromolekulák, monomerjeiket aminosavaknak nevezzük. Az aminosavaknak alapvetően két csoportjuk van:
- nem fehérjeeredetű,
- fehérjeeredetű aminosavak.
A fehérjeeredetű aminosavak szabad állapotban csak kis mennyiségben találhatók meg a sejtekben, főleg fehérjék felépítésében vesznek részt.
Kémiailag amino-karbonsavak, azaz a molekulában két eltérő jellegű funkciós csoport is megtalálható:
- bázisos amino-csoport,
- savas karboxil-csoport.
E kettős jelleg sajátos tulajdonságokat – ikerionos szerkezet, amfoter jelleg – kölcsönöz az aminosavaknak. Minden aminosav egy azonos, és egy eltérő molekula részletből áll:
- az azonos rész tartalmazza az amino-, és a karboxilcsoportokat,
- az eltérő rész az ún. oldallánc, amely szerkezetileg 20 (21) féle lehet.
Az aminosavakat az eltérő oldallánc alapján 4 nagy csoportba osztjuk:
- Apoláris oldalláncú
- glicin (Gly) -H
- alanin (Ala) -CH3
- Poláris oldalláncú aminosavak
- szerin (Ser) -CH2OH
- cisztein (Cys) -CH2SH
- Savas oldalláncú aminosavak
- aszparaginsav (Asp) – CH2COOH
- glutaminsav (Glu) -CH2CH2COOH
- Bázisos oldalláncú aminosavak
- Lizin (Lys) -CH2CH2CH2CH2NH2
A fehérjeeredetű aminosavak ún. alfa aminosavak, mivel a bázisos aminocsoport a karboxilcsoport melletti, ún. alfa szénatomhoz kapcsolódik. Ismertek béta-, ill. gamma aminosavak is, mint pl. a gamma-amino-vajsav (GABA).
Az aminosavak egy részét a szervezet nem, vagy csak elégtelen mennyiségben képes előállítani, ezeket esszenciális aminosavaknak nevezzük, melyeket a táplálékkal kell felvenni. Emberben 9 ilyen aminosav ismert, mint pl. a fenil-alanin, lizin, metionin, valin stb.
Az aminosavak tulajdonságai
Az aminosavak jellegzetes tulajdonságai különös szerkezetükre vezethetők vissza, amelyet döntően a jelenlévő funkciós csoportok határoznak meg.
Szerkezet
Az élő sejtek citoplazmájának megfelelő pH értéken – kb. 7.4 – a molekulában megtalálható két ellentétes funkciós csoport egyaránt megnyilvánul:
- a bázisos -NH2 csoport H+ -t felvéve (+) töltésűvé,
- a savas -COOH csoport H+ -t leadva (-) töltésűvé alakul.
Ennek eredményeképpen a molekulában egyszerre van jelen a két ellentétes töltés. Az ilyen képződményeket ikerionnak nevezzük.
A fizikai tulajdonságaik ionrácsos szerkezetükre vezethetők vissza:
- magas olvadáspontú, szilárd vegyületek,
- vízben általában jól oldódnak, vizes oldatuk az áramot jól vezeti.
Kémiai tulajdonságok
Amfoter vegyületek, azaz savként és bázisként egyaránt viselkedhetnek a reakciópartnertől függően, azonban sav-bázis sajátságaikat az oldallánc kémiai természete is befolyásolja.
Biológiai szempontból legfontosabb reakciójuk a kondenzáció, melynek során az egyik aminosav amino-csoportja, és a másik aminosav karboxil-csoportja között víz kilépéssel, ún. peptidkötés jön létre.
Sarlósejtes vérszegénység
A rendellenesség nevét onnan kapta, hogy a betegek vérében lévő – az egyébként korong alakú – vörösvértestek sarló formájúak. A hibás vörösvértesteket az immunrendszer folyamatosan eltávolítja, aminek következtében csökken a vörösvértestszám (vérszegénység).
A betegség oka az, hogy a vörösvértesteket kitöltő hemoglobin egyik polipeptidláncában az egyik aminosav kicserélődik egy másikra (az egyik béta-láncban a 6. helyen levő Glu helyet Val található). Ennek következtében a hemoglobin oldékonysága megszűnik, kikristályosodik, megváltozik a sejt alakja és oxigénszállítása jelentősen romlik. Genetikai betegség.
Lapozz a további részletekért